ऑक्सीजन है ... ऑक्सीजन फार्मूला ऑक्सीजन अणु
पृथ्वी पर सभी पदार्थों में, एक विशेष स्थान पर कब्जा कर लिया गया हैक्या जीवन प्रदान करता है ऑक्सीजन है यह उनकी उपस्थिति है जो हमारे ग्रह को अन्य सभी लोगों के बीच अद्वितीय बनाता है, विशेष। इस पदार्थ के लिए धन्यवाद, दुनिया में इतने सुंदर जीव हैं: पौधे, जानवर, लोग। ऑक्सीजन एक बिल्कुल अपरिहार्य, अद्वितीय और अत्यंत महत्वपूर्ण परिसर है। इसलिए, यह पता लगाने की कोशिश करें कि यह क्या है, क्या विशेषताएं हैं

रासायनिक तत्व ऑक्सीजन: विशेषता
आरंभ करने के लिए, हम आवधिक तालिका में इस तत्व के स्थान को चिह्नित करते हैं। यह कई वस्तुओं द्वारा किया जा सकता है
- सीरियल नंबर 8 है
- परमाणु द्रव्यमान 15.9 9 0 9 3 है
- यह प्रणाली की दूसरी अवधि के मुख्य उपसमूह के छठे समूह में स्थित है।
- नाभिक का प्रभार 8 है, प्रोटॉन की संख्या 8 है, इलेक्ट्रॉनों की संख्या 8 है, न्यूट्रॉन की संख्या 8 है। इस प्रकार, डबल जादू संख्या प्राप्त की जाती है, जिसके कारण मुख्य समस्थानिक रूप की स्थिरता देखी जाती है 16ओ
- तत्व का लैटिन नाम ऑक्सीजन है। रूसी - ऑक्सीजन, यह नाम "एसिड को जन्म देने" वाक्यांश से बनता है। एक पर्याय भी है, कभी-कभी इसे ऑक्सीजन कहा जाता है
परमाणु की इलेक्ट्रॉनिक संरचना के विश्लेषण के लिए विशेष ध्यान देना चाहिए, क्योंकि यह अणु की स्थिरता और भौतिक और रासायनिक गुणों को प्रदर्शित करता है।
अणु की संरचना
परमाणु का इलेक्ट्रॉनिक कॉन्फ़िगरेशन फॉर्मूला 1 एस द्वारा दर्शाया गया है22s22p4। इस रिकॉर्ड से यह स्पष्ट है कि ऊर्जा स्तर और वाचा ऑक्सेट के निर्माण से पहले ऑक्सीजन में दो इलेक्ट्रॉनों का अभाव है। यह उनकी निम्नलिखित विशेषताएं बताता है:
- ऑक्सीजन अणु डायटोमिक है;
- तत्व की ऑक्सीकरण की डिग्री हमेशा -2 (पेरोक्साइड्स और फ्लोरीन ऑक्साइड को छोड़कर, जिसमें यह क्रमशः -1 और +2 होता है);
- मजबूत ऑक्सीडेंट है;
- सामान्य परिस्थितियों में भी प्रतिक्रिया करना आसान;
- विस्फोटक यौगिकों बनाने में सक्षम है
अब संरचना के सवाल पर विचार करें। ऑक्सीजन अणु कैसे होता है? सबसे पहले, गठन का तंत्र सहसंयोजक गैर-विरल है, अर्थात प्रत्येक परमाणु के इलेक्ट्रॉनों के समाजीकरण के कारण। इस प्रकार, बांड भी सहसंयोजक गैर-पंथ है। इस मामले में, यह दोगुना है, क्योंकि प्रत्येक परमाणु के बाह्य स्तर पर दो अनियोजित इलेक्ट्रॉन होते हैं। आप ऑक्सीजन की तरह दिखते हैं, यह बहुत आसानी से चित्र कर सकते हैं। सूत्र निम्नानुसार है: ओ2 या हे = ओ।
इस तरह के एक बंधन की उपस्थिति के कारण, अणु बहुत स्थिर है उसे शामिल कई प्रतिक्रियाओं के लिए, विशेष परिस्थितियों की आवश्यकता है: बढ़ दबाव, हीटिंग, उत्प्रेरक का उपयोग।
एक रासायनिक तत्व के रूप में, ऑक्सीजन एक परमाणु है,जिसमें तीन आइसोटोप हैं जो प्रकृति में विद्यमान हैं उनकी संख्या क्रमशः 16, 17, 18 है। हालांकि, प्रतिशत अनुपात बहुत अलग है, क्योंकि 16लगभग 99.75 9%, और शेष 0.5% से कम है। इसलिए, सबसे आम और स्थिर आइसोटोप 16 के द्रव्यमान संख्या के साथ सटीक है

साधारण पदार्थ ऑक्सीजन
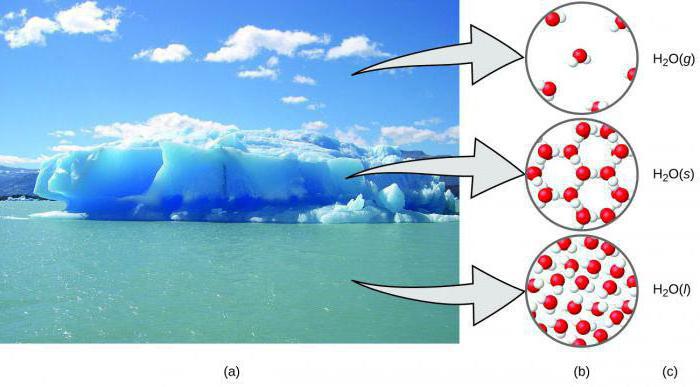
अगर हम इस तत्व के बारे में एक साधारण बात करते हैंकनेक्शन, फिर तुरंत सामान्य स्थिति के तहत कुल राज्य का संकेत मिलता है। ऑक्सीजन एक गैस है जो न तो स्वाद, रंग, न ही गंध है। एक डायटोमिक अणु, जो हाइड्रोजन के बाद ग्रह पर सबसे प्रचुर पदार्थ है और हीलियम के एक महान गैस है।
इस पदार्थ के अन्य समेकन राज्य हैं तो, -183 के नकारात्मक तापमान पर0सी ऑक्सीजन एक खूबसूरत नीली तरल में घुलनशील है। यदि आप -200 के थ्रेसहोल्ड से अधिक हो0सी, तरल एक मोनोकलिनिक सुई की तरह आकार के उज्ज्वल नीले क्रिस्टल में हो जाना होगा।
ठोस राज्य में ऑक्सीजन के तीन मुख्य प्रकार मौजूद हैं।
- अल्फ़ा फॉर्म (α-O2)। 200 से कम तापमान है 0एस
- बीटा फॉर्म (β-O2)। तापमान के अंतराल -200-4000एस
- गामा फॉर्म (γ-O2)। -400 से -500 तक अंतराल0एस
ऑक्सीजन सबसे महत्वपूर्ण और महत्वपूर्ण में से एक हैगैसों। न केवल ग्रह पर जीवित प्राणियों के जीवन के लिए, बल्कि एक संपूर्ण रूप से प्रकृति के लिए। यह एक प्राकृतिक खनिज या परिसर नाम देना मुश्किल है, जिसमें यह एक तत्व के रूप में शामिल नहीं होगा।
खोज का इतिहास
पहला उल्लेख है कि हवा मेंआठवीं शताब्दी में दिखाई देने वाली दहन प्रक्रियाओं का समर्थन करने वाली गैस का कोई प्रकार है। हालांकि, फिर इसे अध्ययन करने के लिए, अस्तित्व को साबित करना और खोलने के लिए कोई तकनीकी संभावना नहीं थी लगभग एक सहस्त्राब्दी के बाद, 18 वीं शताब्दी में यह किया गया था, कई वैज्ञानिकों के काम के लिए धन्यवाद
- 1771 कार्ल शेले ने प्रायोगिक रूप से वायु संरचना की स्थापना की और पाया कि मुख्य दो गैस ऑक्सीजन और नाइट्रोजन हैं।
- पियरे बेएन पारा और उसके आक्साइड के अपघटन पर प्रयोग करता है और आधिकारिक रूप से परिणामों को रिकॉर्ड करता है।
- 1773 शीले ने आधिकारिक रूप से ऑक्सीजन का तत्व खोल दिया है, लेकिन इसे अपने शुद्ध रूप में प्राप्त नहीं करता है।
- 1774 प्रीस्टेली, शेले की परवाह किए बिना, वह करता है वैसे ही करता है, और पारा ऑक्साइड को कमजोर करके शुद्ध ऑक्सीजन मिलता है।
- 1775 एंटीओन लेव्यूज़ियर इस तत्व का नाम देता है और एक दहन सिद्धांत बनाता है जो एक सौ से अधिक वर्षों तक मौजूद है।
- 18 9 8 थॉम्पसन ने सोसायटी को सोचा कि हवा का ऑक्सीजन वातावरण में कार्बन डाइऑक्साइड के बड़े उत्सर्जन के कारण समाप्त हो सकता है।
- उसी वर्ष में तिमिरिज़ेव विपरीत साबित होता है, क्योंकि वह बताते हैं कि ऑक्सीजन के आपूर्तिकर्ता ग्रह के हरे पौधे हैं।
इस प्रकार, यह ज्ञात हो गया कि यहऑक्सीजन का प्रतिनिधित्व करता है, जो महत्वपूर्ण है और जीवन के लिए सार्थक गैस है। पदार्थ के सभी भौतिक और रासायनिक गुणों का अध्ययन किए जाने के बाद, इसे प्राप्त करने के तरीके माना जाता था, पानी की एक अनुमानित सामग्री, पृथ्वी की परत, वातावरण और ग्रह के अन्य स्थानों की गणना की गई थी।

शारीरिक गुण
हम मुख्य भौतिक मापदंडों को देते हैं, जिसके द्वारा इस परिसर की विशेषता हो सकती है।
- ऑक्सीजन सामान्य परिस्थितियों में एक गैस है, जो वायु (21%) का अभिन्न अंग है। इसका कोई रंग, स्वाद और गंध नहीं है हवा से हल्का, पानी में खराब घुलनशील।
- इसे कोयला और धातु पाउडर द्वारा सक्रिय रूप से अवशोषित किया जाता है, यह कार्बनिक पदार्थों में घुल जाता है।
- उबलते बिंदु -183 है0एस
- पिघलने -218.350एस
- घनत्व 0.0014 ग्रा / सेमी है3.
- क्रिस्टल जाली आणविक है
ऑक्सीजन तरल अवस्था में गुणगुणिक गुण हैं।
रासायनिक गुण
प्रश्न में गैस कितनी सक्रिय है, कैसेवह अन्य पदार्थों के साथ प्रतिक्रियाओं में व्यवहार करता है, रसायन विज्ञान विस्तार में बताता है ऑक्सीजन कई डिग्री ऑक्सीकरण प्रदर्शित करने में सक्षम है, हालांकि सबसे लगातार -2 है, जिसे स्थिर माना जाता है इसके अलावा, ऐसे यौगिक हैं जिनमें मूल्य निम्नानुसार हैं:
- -1;
- -0.5;
- -1/3;
- 0.5;
- +1;
- 2।
रासायनिक गतिविधि को उच्च द्वारा समझाया गया हैइलेक्ट्रॉन के प्रति समानता, चूंकि मतदान के अनुसार इलेक्ट्रो-गेटिटिविटी का मूल्य 3.44 है। फ्लोराइड में केवल उच्च (4) इसलिए, ऑक्सीजन एक बहुत मजबूत ऑक्सीडेंट है। इसी समय, अधिक शक्तिशाली ऑक्सीडेंट के साथ प्रतिक्रियाओं में एक सकारात्मक एजेंट के रूप में व्यवहार करता है, जो सकारात्मक ऑक्सीकरण स्थिति का प्रदर्शन करता है। उदाहरण के लिए, फ्लोराइड ऑक्साइड में ओ+2 एफ2- .

इसमें यौगिकों की एक बड़ी संख्या है, जिसमें ऑक्सीजन शामिल है। ये पदार्थों की कक्षाएं हैं, जैसे:
- आक्साइड;
- पेरोक्साइड;
- ozonides;
- सुपरऑक्साइड;
- एसिड;
- आधार;
- नमक;
- जैविक अणुओं
सभी तत्वों के साथ, ऑक्सीजन में प्रवेश करने में सक्षम हैसामान्य परिस्थितियों में प्रतिक्रिया, महान धातुओं, हीलियम, नीयन और आर्गन और हैल्पेंस को छोड़कर। जड़ गैसों के साथ, यह किसी भी परिस्थितियों में बातचीत नहीं करता है
उद्योग में प्राप्त करना
हवा और पानी में ऑक्सीजन सामग्री इतनी बड़ी है (21 और 88% क्रमशः), कि इसके संश्लेषण का मुख्य औद्योगिक तरीका तरल हवा का आंशिक आसवन और पानी के इलेक्ट्रोलिसिस है
पहली विधि विशेष रूप से अक्सर उपयोग किया जाता है। सब के बाद, इस गैस का एक बहुत हवा से अलग किया जा सकता है। हालांकि, यह पूरी तरह से साफ नहीं होगा। यदि उच्च गुणवत्ता वाले उत्पाद की आवश्यकता होती है, तो इलेक्ट्रोलीज़ प्रक्रियाएं शुरू हो जाती हैं। इसके लिए कच्ची सामग्री या तो पानी या क्षार है सोडियम या पोटेशियम हाइड्रॉक्साइड का उपयोग समाधान के विद्युत चालकता को बढ़ाने के लिए किया जाता है। सामान्य तौर पर, इस प्रक्रिया का सार पानी की अपघटन तक कम हो जाता है।

प्रयोगशाला में हो रही है
प्रयोगशाला के तरीकों में, गर्मी उपचार की विधि व्यापक हो गई है:
- पेरोक्साइड;
- ऑक्सीजन युक्त एसिड का लवण
उच्च तापमान पर वे विघटित होते हैंगैसीय ऑक्सीजन की रिहाई इस प्रक्रिया को मैंगनीज (IV) ऑक्साइड द्वारा उत्प्रेरित किया जाता है। ऑक्सीजन को पानी के विस्थापन के द्वारा एकत्र किया जाता है, और यह पाया जाता है - सुगंधित किरण द्वारा। जैसा कि आप जानते हैं, ऑक्सीजन वायुमंडल में, ज्वाला बहुत चमकते हैं।
एक अन्य पदार्थ का उत्पादन होता थास्कूल रसायन विज्ञान के सबक में ऑक्सीजन, - हाइड्रोजन पेरोक्साइड उत्प्रेरक के प्रभाव में भी 3% समाधान तुरंत शुद्ध गैस की रिहाई के साथ decomposes। यह केवल एकत्रित करने की आवश्यकता है उत्प्रेरक एक ही है - मैंगनीज ऑक्साइड MnO2.
सबसे अधिक इस्तेमाल किए गए नमक में ये भी शामिल हैं:
- बर्थलेल्ट्स नमक, या पोटेशियम क्लोरेट;
- पोटेशियम परमैंगनेट, या मैंगनीज
प्रक्रिया का वर्णन करने के लिए, हम समीकरण दे सकते हैं। प्रयोगशाला और अनुसंधान आवश्यकताओं के लिए ऑक्सीजन पर्याप्त है:
2KClO3 = 2 केएल + 3 ओ2↑।
ऑक्सीजन के आलोट्रोपिक संशोधनों
ऑक्सीजन में एक ऑलोट्रोपिक संशोधन है। इस परिसर के लिए सूत्र ओ है3, इसे ओजोन कहा जाता है यह वायु के ऑक्सीजन पर पराबैंगनी और बिजली के निर्वहन के प्रभाव के तहत प्राकृतिक स्थितियों में गठित गैस है। ओ खुद के विपरीत2, ओजोन में ताजगी का सुखद गंध है, जो कि बारिश के साथ बिजली और गरज के साथ हवा में महसूस होता है
ऑक्सीजन और ओजोन के बीच का अंतर अणु में परमाणुओं की संख्या ही नहीं है, बल्कि क्रिस्टल जाल के ढांचे में भी है। रासायनिक रूप से, ओजोन एक भी मजबूत ऑक्सीडिजर है
ऑक्सीजन हवा का एक घटक है
प्रकृति में ऑक्सीजन का वितरण बहुत व्यापक है ऑक्सीजन पाया जाता है:
- चट्टानों और खनिजों;
- पानी नमकीन और ताजा;
- मिट्टी;
- पौधे और पशु जीव;
- ऊपरी वायुमंडल सहित हवा
जाहिर है, पृथ्वी के सभी गोले इसके द्वारा कब्जा कर रहे हैं -लिथोस्फीयर, जलमंडल, वायुमंडल और जीवमंडल विशेष रूप से महत्वपूर्ण हवा में इसकी सामग्री है सब के बाद, यह इस पहलू है कि हमारे ग्रह पर मौजूद मनुष्यों सहित जीवन रूपों की अनुमति देता है।

हम जो हवा की सांस लेते हैं वह बहुत विषम है। इसमें लगातार घटकों और चर दोनों शामिल हैं अपरिवर्तित और हमेशा उपस्थित हैं:
- कार्बन डाइऑक्साइड;
- ऑक्सीजन;
- नाइट्रोजन;
- महान गैसों
चर में जल वाष्प, धूल कण, बाहरी गैसों (निकास, दहन उत्पादों, सड़ांध, आदि), पौधे पराग, बैक्टीरिया, कवक और अन्य शामिल हैं।
प्रकृति में ऑक्सीजन का महत्व
यह बहुत महत्वपूर्ण है कि ऑक्सीजन कितना हैप्रकृति। यह ज्ञात है कि बड़े ग्रहों (बृहस्पति, शनि) के कुछ उपग्रहों पर इस गैस की मात्रा का पता चला था, लेकिन वहां कोई स्पष्ट जीवन नहीं है। हमारी धरती में पर्याप्त संख्या है, जो पानी के संयोजन के साथ सभी जीवों के लिए संभव है।
साँस लेने में सक्रिय भागीदार होने के अलावा, ऑक्सीजन अभी भी अनगिनत ऑक्सीकरण प्रतिक्रियाओं का आयोजन करता है, जो जीवन के लिए ऊर्जा जारी करता है।
इस अद्वितीय गैस के मुख्य आपूर्तिकर्ता हैंप्रकृति हरी पौधों और कुछ प्रकार के बैक्टीरिया हैं उनके लिए धन्यवाद, ऑक्सीजन और कार्बन डाइऑक्साइड का निरंतर संतुलन बनाए रखा जाता है। इसके अलावा, ओजोन संपूर्ण पृथ्वी पर एक सुरक्षात्मक ढाल बनाता है, जो कि इसे नष्ट करने वाले पराबैंगनी विकिरण की मात्रा में प्रवेश की अनुमति नहीं देता है

केवल कुछ प्रकार के एनारोबिक जीव (बैक्टीरिया, कवक) ऑक्सीजन वायुमंडल के बाहर रहने में सक्षम हैं। हालांकि, उन लोगों की तुलना में उनमें से बहुत कम हैं जिनके लिए इसकी आवश्यकता है।
उद्योग में ऑक्सीजन और ओजोन का उपयोग
उद्योग में एलोोट्रोपिक ऑक्सीजन संशोधनों के उपयोग के मुख्य क्षेत्र इस प्रकार हैं:
- धातुकर्म (वेल्डिंग और काटने धातुओं के लिए)
- चिकित्सा।
- कृषि।
- रॉकेट ईंधन के रूप में
- विस्फोटकों सहित कई रासायनिक यौगिकों के संश्लेषण
- शुद्धि और पानी की कीटाणुशोधन
यहां तक कि एक प्रक्रिया को नाम देना मुश्किल है जिसमें यह महान गैस, एक अनोखा पदार्थ - ऑक्सीजन भाग नहीं लेते।
</ p>